Casa dos Resumos

Fórmula de Lewis ou Fórmula Eletrônica

Fórmula de Lewis
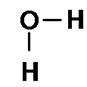
Fórmula Estrutural
- Modelo Atômico
Teoria Atômica - Demócrito: Ele era discípulo de Leucipo, Demócrito dizia que se dividíssemos uma matéria (independente de qual fosse) acharíamos o átomo, este é uma porção indivisível da matéria. - Dalton: Também dizia que o átomo...
- A Estrutura Do átomo
A estrutura do átomo O átomo tem como composição os elétrons, prótons e nêutrons. Os prótons tem carga positiva, os elétrons têm carga negativa e os nêutrons como o próprio nome diz não tem carga. Referente ao peso o elétron tem peso quase...
- Modelo Atômico
Modelo atômico O conceito de átomo começou antes de cristo quando Demócrito disse que toda matéria era construída por partículas minúsculas, individuais denominadas átomos. Os principais modelos: O modelo de John Dalton ? bola de bilhar-1808:...
- Quimica
Cátions e ânions são íons (átomos ou moléculas que perderam ou ganharam elétrons). Cátions têm carga positiva e ânions carga negativa. Por que isso? Simples: Alguns átomos, para se tornarem estáveis, liberam ou ganham elétrons, até que sua...
- Química I
DISTRIBUIÇÃO ELETRÔNICA LIGAÇÕES QUIMICAS *Os elementos querem imitar os gases nobres, ou seja, ter 8 elétrons na última camada (estabilidade) * os outros elementos para adquirir estabilidade doam ou compartilham elétrons, fazendo ligações...
Casa dos Resumos
Ligação Covalente
LIGAÇÃO COVALENTE
A ligação covalente, geralmente é feita entre os não-metais e não metais, hidrogênio e não-metais e hidrogênio com hidrogênio.
Esta ligação é caracterizada pelo compartilhamento de elétrons. O hidrogênio possui um elétron na sua camada de valência. Para ficar idêntico ao gás nobre hélio com 2 elétrons na última camada. Ele precisa de mais um elétron. Então, 2 átomos de hidrogênio compartilham seus elétrons ficando estáveis:
Esta ligação é caracterizada pelo compartilhamento de elétrons. O hidrogênio possui um elétron na sua camada de valência. Para ficar idêntico ao gás nobre hélio com 2 elétrons na última camada. Ele precisa de mais um elétron. Então, 2 átomos de hidrogênio compartilham seus elétrons ficando estáveis:
Ex. H (Z = 1) K = 1
H ? H ? H2
O traço representa o par de elétrons compartilhados.
Nessa situação, tudo se passa como se cada átomo tivesse 2 elétrons em sua eletrosfera. Os elétrons pertencem ao mesmo tempo, aos dois átomos, ou seja, os dois átomos compartilham os 2 elétrons. A menor porção de uma substância resultante de ligação covalente é chamada de molécula. Então o H2 é uma molécula ou um composto molecular. Um composto é considerado composto molecular ou molécula quando possui apenas ligações covalentes
Observe a ligação covalente entre dois átomos de cloro:

Fórmula de Lewis ou Fórmula Eletrônica
Cl ? Cl
Fórmula Estrutural
Fórmula Estrutural
Cl 2
Fórmula Molecular
Fórmula Molecular
Conforme o número de elétrons que os átomos compartilham, eles podem ser mono, bi, tri ou tetravalentes.
A ligação covalente pode ocorrer também, entre átomos de diferentes elementos, por exemplo, a água.

Fórmula de Lewis

Fórmula Estrutural
H2O
Fórmula Molecular
Fórmula Molecular
A água, no exemplo, faz três ligações covalentes, formando a molécula H2O. O oxigênio tem 6é na última camada e precisa de 2é para ficar estável. O hidrogênio tem 1 é e precisa de mais 1é para se estabilizar. Sobram ainda dois pares de elétrons sobre o átomo de oxigênio.
A ligação covalente pode ser representada de várias formas.
As fórmulas em que aparecem indicados pelos sinais . ou x são chamadas de fórmula de Lewis ou fórmula eletrônica.
Quando os pares de elétrons são representados por traços (-) chamamos de fórmula estrutural plana, mostrando o número de ligações e quais os átomos estão ligados.
A fórmula molecular é a mais simplificada, mostrando apenas quais e quantos átomos têm na molécula.
Veja o modelo:
A ligação covalente pode ser representada de várias formas.
As fórmulas em que aparecem indicados pelos sinais . ou x são chamadas de fórmula de Lewis ou fórmula eletrônica.
Quando os pares de elétrons são representados por traços (-) chamamos de fórmula estrutural plana, mostrando o número de ligações e quais os átomos estão ligados.
A fórmula molecular é a mais simplificada, mostrando apenas quais e quantos átomos têm na molécula.
Veja o modelo:
H . . H H ? H H2
Fórmula de Lewis ou eletrônica Fórmula Estrutural Plana Fórmula Molecular
loading...
- Modelo Atômico
Teoria Atômica - Demócrito: Ele era discípulo de Leucipo, Demócrito dizia que se dividíssemos uma matéria (independente de qual fosse) acharíamos o átomo, este é uma porção indivisível da matéria. - Dalton: Também dizia que o átomo...
- A Estrutura Do átomo
A estrutura do átomo O átomo tem como composição os elétrons, prótons e nêutrons. Os prótons tem carga positiva, os elétrons têm carga negativa e os nêutrons como o próprio nome diz não tem carga. Referente ao peso o elétron tem peso quase...
- Modelo Atômico
Modelo atômico O conceito de átomo começou antes de cristo quando Demócrito disse que toda matéria era construída por partículas minúsculas, individuais denominadas átomos. Os principais modelos: O modelo de John Dalton ? bola de bilhar-1808:...
- Quimica
Cátions e ânions são íons (átomos ou moléculas que perderam ou ganharam elétrons). Cátions têm carga positiva e ânions carga negativa. Por que isso? Simples: Alguns átomos, para se tornarem estáveis, liberam ou ganham elétrons, até que sua...
- Química I
DISTRIBUIÇÃO ELETRÔNICA LIGAÇÕES QUIMICAS *Os elementos querem imitar os gases nobres, ou seja, ter 8 elétrons na última camada (estabilidade) * os outros elementos para adquirir estabilidade doam ou compartilham elétrons, fazendo ligações...
